 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Представники гомологічного ряду алканів
Таблиця 9.1
V 0,154 нм\0,110 нм А б в Рис. 9.1. Будова молекули етану: а — кулестрижнева модель; б — геометрія молекули; в — о-зв'язки Навколо вуглець-вуглецевих зв'язків відбувається вільне обертання, у результаті якого молекула може приймати різні просторові форми — конформації (рис. 9.2).
І'"/ Рис. 9.2. Конформації алканів: а — зиґзаґоподібна; б — нерегулярна; в — клішнеподібна АЛІФатиЧнІ ВУГЛеВОДнІ. аЛКани
НОМЕНКЛАТУРА Перші чотири представники гомологічного ряду алканів мають тривіальні назви — метан, етан, пропан, бутан. Назва наступних вуглеводнів з нормальним вуглецевим ланцюгом утворюється від назви грецького числівника, яка вказує кількість атомів Карбону в молекулі, з додаванням суфікса -ан: пентан, гексан тощо (див. табл. 9.1). У назвах алканів з розгалуженим ланцюгом, в яких дві метильні групи знаходяться на одному кінці вуглецевого ланцюга, що не має інших відгалужень, використовується префікс ізо-, якщо ж на кінці вуглецевого ланцюга є три метильні групи, у назву алкана вводиться префікс нео-: СН сн3—сн2—сн2—сн сн3—сн2—с—сн3 СН3 ізогексан неогексан Назви алканів з розгалуженим вуглецевим ланцюгом складають за замісниковою номенклатурою ШРАС: 1. За основу приймають назву вуглеводню, якому відповідає найдовший не-розгалужений вуглецевий ланцюг (головний вуглецевий ланцюг). якщо у вуглеводні є кілька ланцюгів однакової довжини, то головним з них вважається той, що має найбільшу кількість розгалужень:
сн3'——^------ ' сн3 ' сн3—сн—сн—сн2—сн3 сн3—сн—сн—сн2—сн3 2. Нумерують атоми Карбону головного ланцюга з того кінця, до якого ближче розташований замісник. якщо в молекулі алкану замісники розміщені на рівній відстані від обох кінців, то нумерацію починають з того кінця, до якого ближче знаходиться замісник з назвою, що стоїть за алфавітним порядком раніше: 54321 1234567 сн3—сн2—сн2—сн—сн3 сн3—сн2—сн—сн2—сн—сн2—сн3 СН3 СН2 СН3 СН3 2-метилпентан З-етил-5-метилгептан Глава 9 128 Г якщо ж на однаковій відстані від обох кінців головного ланцюга розташовані ідентичні замісники, але з одного боку кількість розгалужень більша, ніж з іншого, нумерацію починають з того кінця, де більша кількість замісників: СН3 сн3—с—сн2—сн2—сн—сн3 сн3—сн—сн2—сн—сн—сн3 СН3 СН3 СН3 СН3 СН3 2,2,5-триметилгекоан 2,3,5-триметилгекоан 3. Складають назву сполуки в цілому, дотримуючись певних правил: а) спочатку перелічують за алфавітним порядком назви замісників, указуючи б) потім називають вуглеводень, якому відповідає головний вуглецевий ланцюг Замісниками при головному вуглецевому ланцюзі в алканах є одновалентні залишки алканів, так звані алкільні групи, або алкільнірадикали; їх позначають Аlk або R. Назви алкільних груп утворюють з назв відповідних алканів, замінюючи суфікс -ан на -ил (-іл). Найчастіше зустрічаються алкільні радикали: _ _ _ _ СНзХ СН3 СН3 СН2 СН3 СН2 СН2 уСН— сн/ метил етил пропіл ізоопропіл СН3 снзЧ І сн3—сн2—сн2—сн2— рсн—сн2— сн3—сн2—сн— сн3—с— СН3 СН3 СН3 бутил ізобутил втор-бутил трет-бутил У наведених назвах префікси втор- (вторинний) і трет- (третинний) характеризують атом Карбону з вільною валентністю. Для назви складних розгалужених радикалів використовують нумерацію вуглецевого ланцюга радикала, причому починають нумерацію завжди з атома Карбону, який має вільну валентність: 5 4 3 2 1 сн3—сн—сн—сн2—сн2— СН3 СН3 3,4-диметилпентил Назви залишків молекул алканів, які мають дві вільні валентності, утворюють від назв відповідних алканів шляхом заміни суфікса -ан на -илен (-ілен) (якщо вільні валентності знаходяться при різних атомах Карбону) або -иліден (-іліден) (якщо вільні валентності знаходяться біля одного і того ж атома Карбону): аЛІФатиЧнІ ВУГЛеВОДнІ. аЛКани
—сн2— метилен -сн2—сн2- сн3—сн= сн3—сн2—сн= пропіліден
СН3— С— СН3 —СН—сн2— сн, СН2 СН2 СН2
ізопропіліден пропілен триметилен Зважаючи на розглянуті правила складання назв алканів за замісниковою номенклатурою ШРАС, нижченаведені вуглеводні слід називати таким чином:
СН3—сн2—С— СН3 2,2-диметилбутан сн 1 2 31 4 5| 6 7 8 сн3—сн—сн—сн2—с—сн2—сн2—сн3 С-ГІ2 5-етил-3-ізопропіл-2,5-диметилоктан ІЗОМЕРІЯ Для алканів характерна структурна та оптична ізомерії. Структурна ізомерія алканів зумовлена різною послідовністю зв'язування атомів Карбону в молекулі (ізомерія ланцюга). Вона характерна для бутану і наступних гомологів ряду алканів:
С4Н -сГІі 2 СН3— СН чсн3 ізобутан; 2-метилпропан СН3 СН3— С— СН3 СН3
ізопентан; 2 -метилб утан неопентан; 2,2-диметилпропан Зі збільшенням кількості атомів Карбону в молекулі алкана кількість структурних ізомерів значно зростає. Так, гексан С6Н14 має п'ять ізомерів, гептан С7Н16 — дев'ять, октан С8Н18 — 18, декан С10Н22 — 75, ейкозан С20Н42 — 366319. Для алканів, починаючи з вуглеводню складу С7Н16, можлива оптична ізомерія. Так, 3-метилгексан СН3СН2С*Н(СН3)СН2СН2СН3 має асиметричний атом Карбону і існує у вигляді двох енантіомерів (дзеркальних ізомерів): СН, Сн,
сн3—сн2 ■'«/ тт
у * о С-ГІ2 С-ГІ2 чсн2—сн3
S- 3 -метилгексан Глава 9
ПРИРОДНІ ДЖЕРЕЛА Головними природними джерелами алканів є нафта і природний газ. Нафта — це складна суміш органічних сполук, основними компонентами якої є нерозгалу-жені і розгалужені алкани. Природний газ складається з газоподібних алканів — переважно метану (до 95%), етану, пропану і бутану. Для одержання суміші алканів та інших вуглеводнів нафту піддають фракційній перегонці. У результаті перегонки виділяють кілька фракцій (петролейний ефір, бензин, гас, дизельне пальне, мазут), кожна з яких становить суміш вуглеводнів, що киплять у певному інтервалі температур (табл. 9.2). Таблиця 9.2 Фракції, які одержують перегонкою нафти
З мазуту перегонкою під вакуумом або з водяною парою добувають солярове масло (вуглеводні складу С18—С25), мастила (вуглеводні складу С28—С38), вазелін і парафін. Подальшою перегонкою фракцій нафти можна одержати індивідуальні алкани. Природний газ розділяють на складові компоненти шляхом зрідження з подальшою фракційною перегонкою.
Поиск по сайту: |



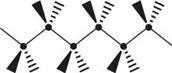
 На підставі даних рентгеноструктурного аналізу встановлено, що алкани нормальної (нерозгалуженої) будови в кристалічному стані мають зиґзаґоподібну конформацію. Така будова для молекули найбільш вигідна, оскільки в цьому разі всі атоми Карбону відносно один одного перебувають у загальмованій антибута-новій конформації. При розгалуженій будові вуглецевого ланцюга конформація може змінюватися.
На підставі даних рентгеноструктурного аналізу встановлено, що алкани нормальної (нерозгалуженої) будови в кристалічному стані мають зиґзаґоподібну конформацію. Така будова для молекули найбільш вигідна, оскільки в цьому разі всі атоми Карбону відносно один одного перебувають у загальмованій антибута-новій конформації. При розгалуженій будові вуглецевого ланцюга конформація може змінюватися.
 головний ланцюг ланцюг не є головним
головний ланцюг ланцюг не є головним R-3 -метилгексан
R-3 -метилгексан 9.4. СПОСОБИ ДОБУВАННЯ
9.4. СПОСОБИ ДОБУВАННЯ